9月2日,CDE官网显示,华东医药递交了利拉鲁肽注射液的上市申请并获承办。这是首款报产的国产利拉鲁肽生物类似药。点击查看受理号详情
利拉鲁肽(liraglutide,1)是人胰高血糖素样肽1(glucagon-like peptide-1,GLP-1)的类似物,是糖尿病治疗的重要靶点,具有多种生理功能:血糖依赖性促进胰岛素分泌、保护胰岛β细胞、延迟胃排空降低食欲等。在全球糖尿病市场上,GLP-1仅次于胰岛素位居第二,2020年的市场总规模达到124亿美元,并且呈现高速增长,加速实现胰岛素替代,大有后者居上之势。
利拉鲁肽原研产品由丹麦诺和诺德公司(NovoNordisk)研发,于2010年在美国上市,商名为Victoza;减肥适应症于2014年12月获批,商品名为Saxenda。2011年,利拉鲁肽以诺和力为商品名获批进入了中国市场,在2017年通过谈判进入医保之后销售额大增,根据诺和诺德财报,2020年全球销售额187.47亿丹麦克朗(-14.5%),其中中国区贡献10.33亿丹麦克朗(+15%)。
利拉鲁肽(Victoza)历年销售额趋势
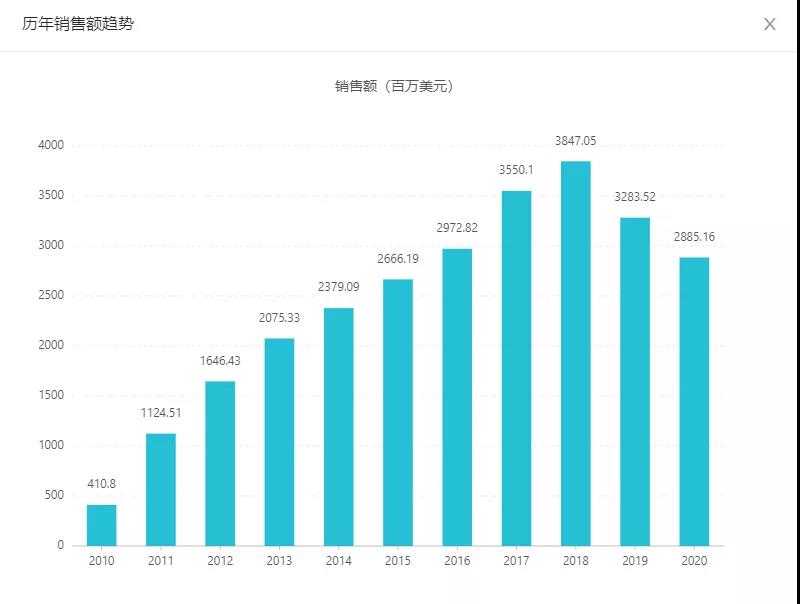
来自Insight数据库(http://db.dxy.cn/v5/home/)
Insight数据库显示,目前国内已获批的GLP-1受体激动剂主要有8个,分别是短效制剂艾塞那肽(百泌达)、贝那鲁肽(谊生泰)、利拉鲁肽(诺和力)和利司那肽(利时敏);长效抑制剂洛塞那肽(孚来美)、艾塞那肽微球(百达杨)、度拉糖肽(度易达)、司美格鲁肽(诺和泰),其中司美格鲁肽在今年4月刚刚获批。从市场份额来看,目前利拉鲁肽是国内GLP-1当之无愧的王者,不过司美格鲁肽的上市无疑将带来较大威胁,在全球市场上,司美格鲁肽已完成对利拉鲁肽的反超。
次华东医药的利拉鲁肽申报上市,成为了国产首家申报上市的利拉鲁肽类似药。不过,这一品种竞争激烈,还有7家已经进入III期临床,包括通化东宝、正大天晴、东阳光、珠海联邦、万邦生化等;5家启动了I期临床或BE试验。
利拉鲁肽注射液国内竞争格局(Insight)
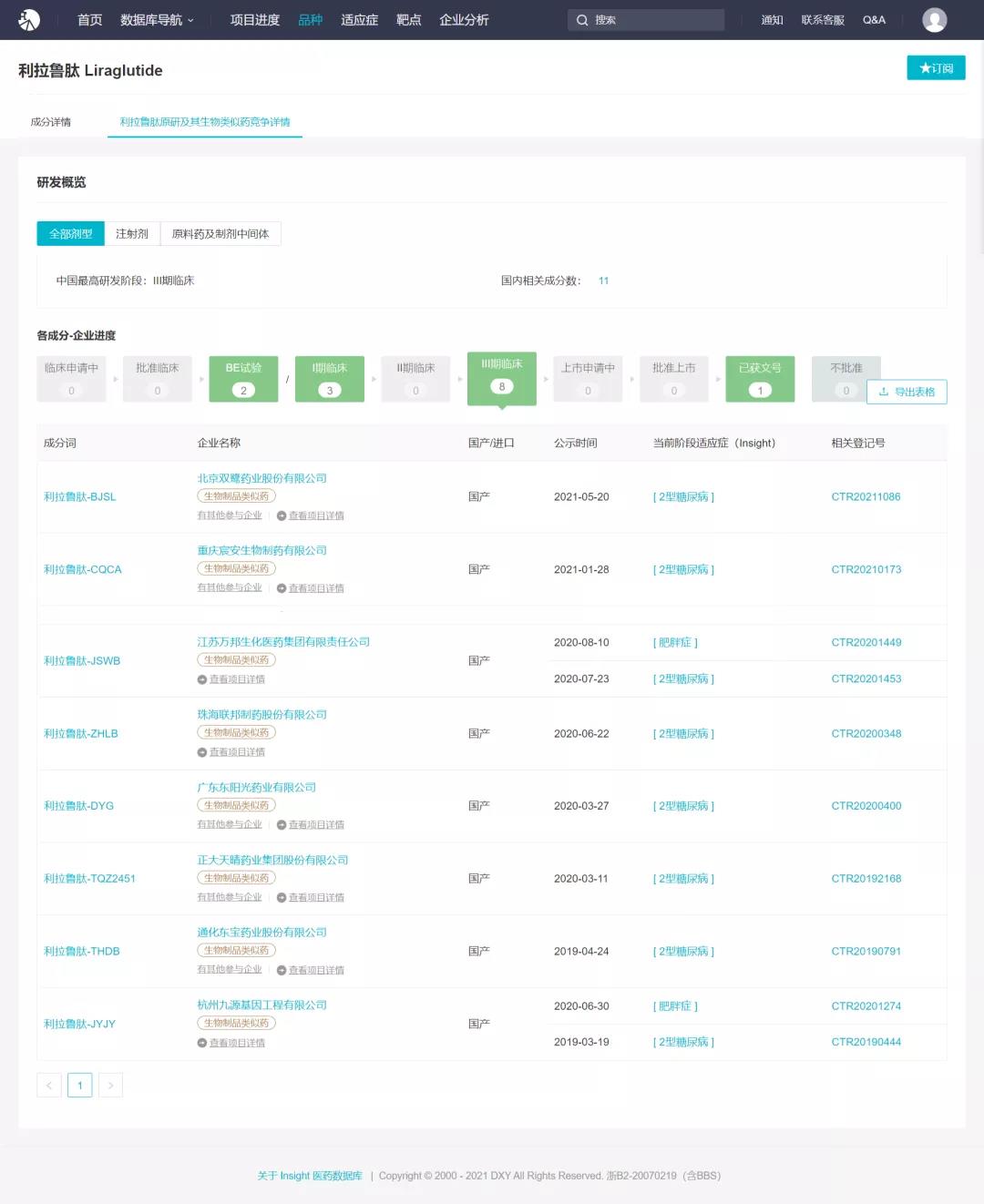
来自Insight数据库(http://db.dxy.cn/v5/home/)
糖尿病领域是华东医药持续深耕的重点领域之一。此前,由于华东医药管线中糖尿病产品仿制药所占比例极大,受集采影响较大,因此华东如今已经开始深入布局生物类似药和创新药,以加强糖尿病管线实力。
在GLP-1生物类似药方面,本次利拉鲁肽注射剂2型糖尿病适应症率先报产,后续减肥适应症也紧随其后。据此前华东半年报披露,减肥适应症也在国内开展3期临床,预计在2021年内也将提交注册申请。
华东医药还和参股公司重庆派金合作开发索马鲁肽注射剂(即司美格鲁肽),目前正在开展动物试验,计划在2021年内启动中国临床试验申请(IND)的申报。司美格鲁肽目前国内尚未有企业进入临床,珠海联邦和九源基因两家已经递交了IND申请。
引进创新药项目方面,2017年华东医药从美国vTv公司引进了口服GLP-1受体激动剂小分子创新药TTP273片,为全球首款,用于治疗2型糖尿病。目前国内上市的GLP-1以注射剂为主,TTP273作为口服药物具有依从性优势,同时兼具成本优势。当前,TTP273正在开展2期中国大陆、台湾多中心临床试验,预期今年年底前结束2期临床,2022年正式进入3期临床。
2021年6月华东医药还引进了日本SCOHIA PHARMA,Inc.临床I期在研产品SCO-094,该产品为GLP-1R和GIPR靶点的双重激动剂,用于治疗2型糖尿病、肥胖和非酒精性脂肪性肝炎(NASH)等疾病。
本文为转载,仅做分享之用,对文章观点保持中立,如侵删。


