2021年08月26日,赛生药业申报的那昔妥单抗注射液上市申请已被中国国家药监局药品审评中心(CDE)纳入拟优先审评,拟开发用于治疗复发性或难治性高危神经母细胞瘤患者。
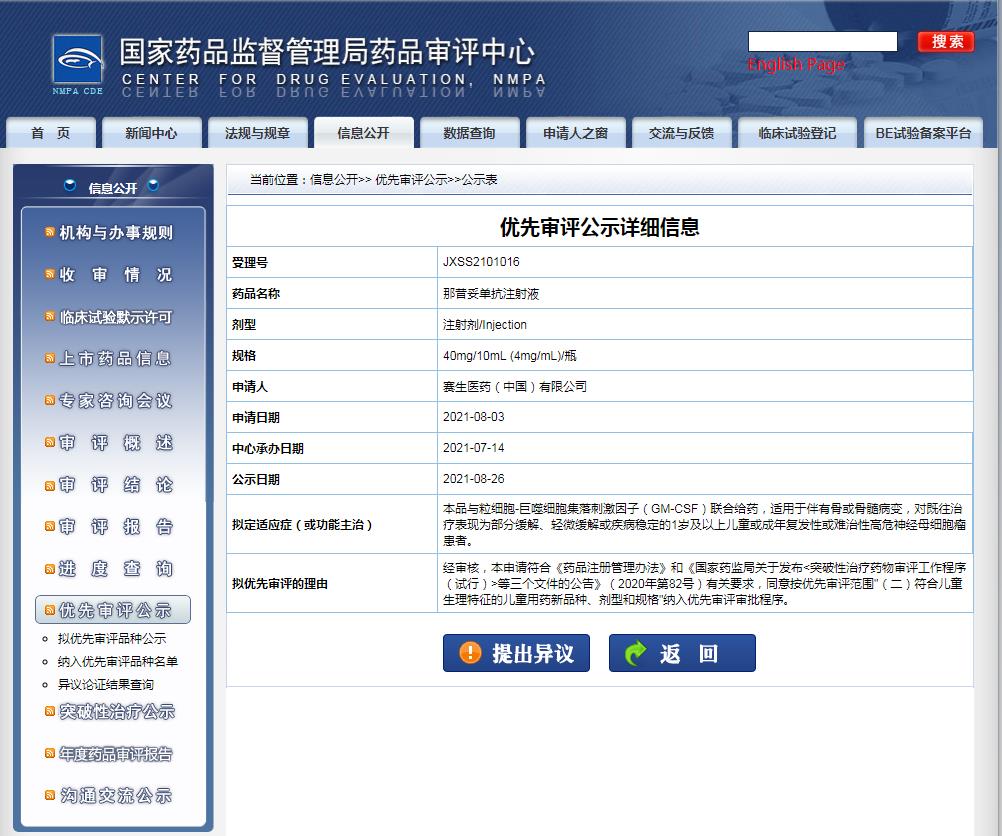
截图来源:CDE官网
那昔妥单抗是Y-mAbs Therapeutics(以下简称“Y-mAbs”)开发的一款靶向神经节苷脂(GD2)的人源化单克隆抗体。GD2抗原在各种神经外胚层生成的肿瘤表面呈现高表达,包括神经母细胞瘤、黑色素瘤和骨肉瘤等肿瘤。
公开资料显示,赛生药业与其原研药企Y-mAbs公司在2020年12月达成了授权许可协议,获得了两款产品在大中华地区(包括中国大陆、香港、澳门和台湾地区)的开发和商业化权利。一款是那昔妥单抗,另外一款产品是omburtamab,拟开发适应症为:用于治疗儿童中枢神经系统/软脑膜转移的神经母细胞瘤。
据悉,在2020年11月获得美国FDA的加速批准之前,那昔妥单抗曾获得美国FDA授予的优先审批资格、突破性疗法认定以及孤儿药资格。
2021年7月,中国国家药品监督管理局(NMPA)受理赛生药业与Y-mAbs公司联合递交那昔妥单抗的上市许可申请(BLA),这次申请的适应症:与粒细胞-巨噬细胞集落刺激因子(GM-CSF)联合给药,用于治疗伴有骨或骨髓病变,对既往治疗表现为部分缓解、轻微缓解或疾病稳定的1岁及以上儿童,或者成年复发性或难治性高危神经母细胞瘤患者。
关于神经母细胞瘤
神经母细胞瘤一直以来被称作“儿童肿瘤之王”,这种肿瘤占所有儿童肿瘤的8%—10%[1],其常见的发病部位是肾上腺,但是也可以发生于颈部、胸部、腹部以及盆腔的神经组织。
因为原发部位隐匿、容易转移,早期确诊会比较困难,确诊时的中位年龄为 17~18 个月,约一半患儿确诊时即处于高危状态[1],[2]。高危神经母细胞瘤患儿在经过综合治疗之后,预后依然比较差,长期生存率不足50%[3]。
现如今,用于神经母细胞瘤儿童患者的药物,主要包括两种,分别为化疗药物和免疫治疗药物,在国内目前还没有针对高危神经母细胞瘤的免疫治疗药物获批上市,患者还远远不能满足对这类疗法的需求。
期待那昔妥单抗尽早在国内获批,给高危神经母细胞瘤患者带来新的希望。
参考文献:
[1]田永帅等;;神经母细胞瘤免疫治疗研究进展[J];现代生物医学进展;2015年10期
[2]"Treatment and outcomes of 1041 pediatric patients with neuroblastoma who received multidisciplinary care in China." Pediatric Investigation 4.3(2020).
[3]Pinto NR, et al. Advances in Risk Classification and Treatment Strategies for Neuroblastoma. J Clin Oncol. 2015; 33(27): 3008-3017.
