2021年12月8日,先声药业注射用曲拉西利(Trilaciclib)的上市申请(受理号:JXHS2101087)被中国国家药品监督管理局药品审评中心(CDE)按“符合附条件批准的药品”拟纳入优先审评审批程序。
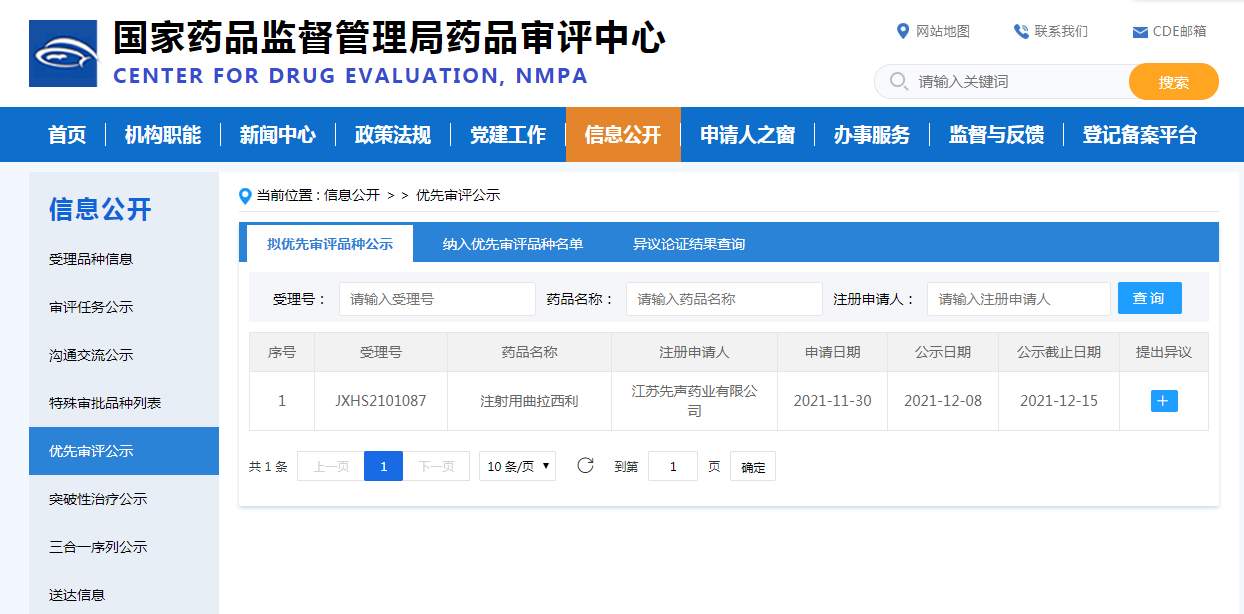
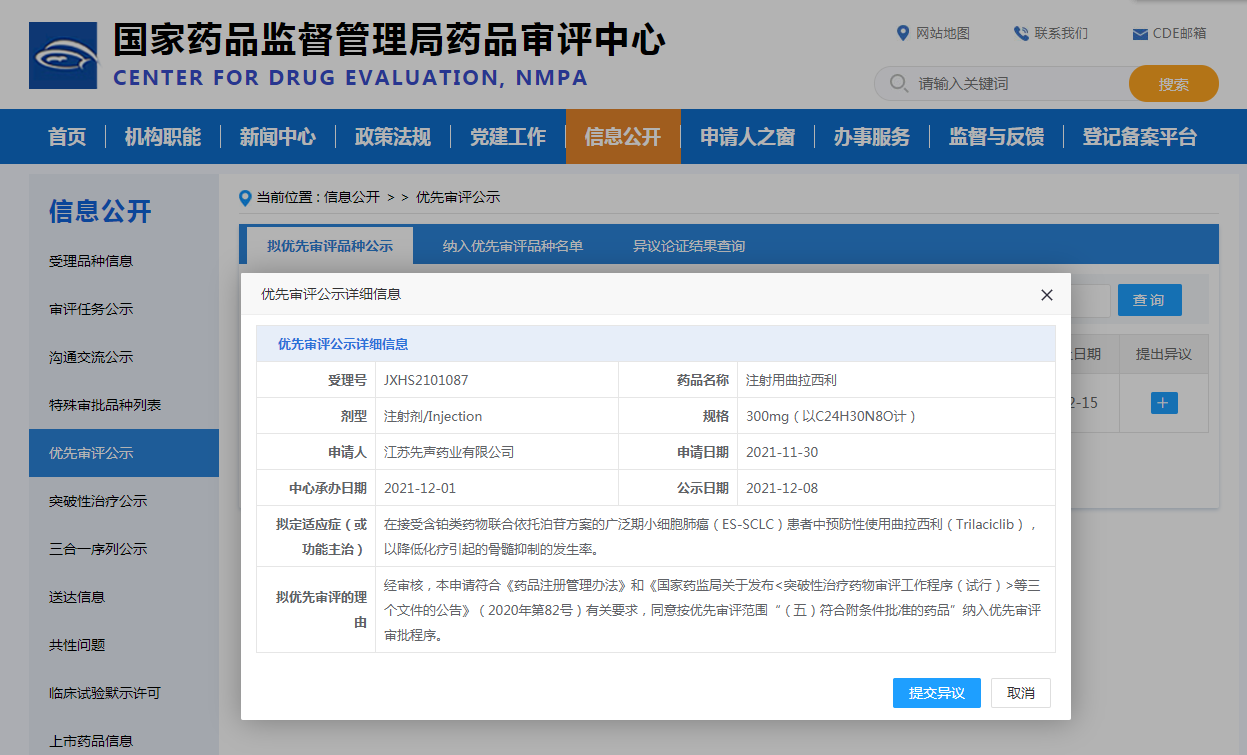
截图来源:CDE官网
拟定适应症(或功能主治):在接受含铂类药物联合依托泊苷方案的广泛期小细胞肺癌(ES-SCLC)患者中预防性使用曲拉西利,以降低化疗引起的骨髓抑制的发生率。
曲拉西利是一款细胞周期蛋白依赖性激酶4/6(CDK4/6)抑制剂,由G1 Therapeutics开发。
曲拉西利是先声药业在 2020 年 8 月从G1 Therapeutics引进的。在美国,曲拉西利曾获FDA授予的突破性疗法认定和优先审评资格,并已于2021年2月获得FDA批准上市,这项批准基于3项随机双盲、安慰剂对照的II期临床试验。商品名为COSELA™,用于治疗小细胞肺癌和化疗引起的骨髓抑制。
值得一提的是,基于先声药业与G1 Therapeutics在境内外开展的多项临床研究的结果,先声药业在中国提交了曲拉西利的上市申请。
关于骨髓抑制
根据GLOBOCAN2018显示,全球恶性肿瘤新发病例约1 808万例,死亡病例约956万例,中国分别约占23.7%和30%[1]。肿瘤已成为慢性病之一,严重影响人们的健康。
可能需要进行药物治疗的肿瘤患者大约超过一半,就目前的发展水平来讲,化疗仍然是药物治疗中不可被完全替代的治疗手段。作为基础治疗手段的化疗,由于癌细胞本身是体内细胞的变异,化疗不能加以区分,因此骨髓中产生的白细胞、红细胞和血小板等细胞在一定程度上受到了影响,可引起有不同程度的骨髓抑制副反应,进而造成患者出现感染、贫血、自发性出血、休克情况严重时甚至死亡,同时生存期缩短、生活质量降低。
骨髓抑制一旦发生,需要进行医疗干预,例如通过输血、注射生长因子或输血小板,但这些方法针对的是某一类血细胞,而且可能会带来一系列额外的风险。而且,同时往往需要降低药物剂量或中断治疗,影响患者的生存获益。一直以来,骨髓抑制缺乏新的疗法和预防手段,因此,存在迫切的医疗需求。
参考文献:
[1] Ferlay J, Ervik M, Bray F, et al. Global Cancer Observatory: Cancer Today. Lyon, France: International Agency for Research on Cancer [EB/OL]. https://gco.iarc.fr/today.
