4月19日,中国国家药监局(NMPA)药品注册进度查询结果显示,诺和诺德(Novo Nordisk)提交的司美格鲁肽注射液新药上市申请办理状态已更新为“待审批”。这意味着,这款GLP-1类似物在中国的注册进度又进一步。若顺利获批,它将为中国2型糖尿病患者带来全新的治疗选择。
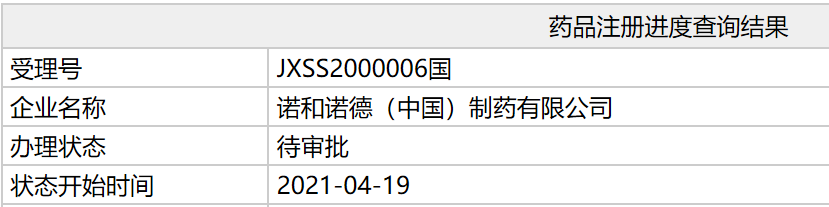
截图来源:NMPA官网
2型糖尿病是一种严重的疾病。这种疾病往往是因为人体无法产生足够的胰岛素,或是无法正确利用人体合成的胰岛素所致。因此,这些患者的血糖调控能力会受到很大的影响。不幸的是,罹患2型糖尿病的患者与健康人相比,出现心血管疾病的风险要高出2-4倍。作为一种影响终生的疾病,2型糖尿病急需治疗和控制手段。
司美格鲁肽(semaglutide)是一种胰高糖素样肽-1(GLP-1)类似物,能起到GLP-1受体激动剂的作用,并且能为患者带来心血管代谢获益。此前,该产品已经在美国被FDA批准用于成人2型糖尿病治疗,以及用于降低2型糖尿病和合并心血管疾病成人2型糖尿病患者的主要心血管不良事件(MACE)风险。公开资料显示,司美格鲁肽通过突破性的肽链结构优化,使得分子半衰期延长至7天,实现了一周一次给药且血药浓度平稳。
根据诺诺德近期发布的SUSTAIN China研究结果,该研究是司美格鲁肽在中国的注册临床试验,是一项以中国人群为主的多国家、多中心3期临床试验,在二甲双胍基础上对比了司美格鲁肽与对照药物的治疗疗效和安全性。研究纳入了868名2型糖尿病患者,主要终点为30周时HbA1c自基线的变化。
此次司美格鲁肽在中国上市申请审评审批状态进入待审批,意味着这款产品距离在中国获批又进一步。希望它能早日获批,让更多中国糖尿病患者也能获益。
注:本文为载,仅做分享之用,对文章观点保持中立,侵权即删。
注:本文为载,仅做分享之用,对文章观点保持中立,侵权即删。
