2021年6月9日,中国国家药品监督管理局(NMPA)公示,由荣昌生物制药(烟台)股份有限公司自主研发的注射用维迪西妥单抗(商品名:爱地希)适用于至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌(包括胃食管结合部腺癌)患者的治疗的新药上市申请正式获批。
.jpg)
截图来源:NMPA官网
关于维迪西妥单抗
维迪西妥单抗是中国公司开发的一款靶向HER2的抗体偶联药物,现被开发用于治疗目前尚缺乏治疗手段的常见HER2表达适应症,包括:HER2低表达的癌症(IHC 2+/FISH-或IHC 1+)适应症,例如HER2低表达的乳腺癌;以及乳腺癌以外的HER2表达(IHC 1+或以上)癌症适应症,例如胃癌和尿路上皮癌。
.jpg)
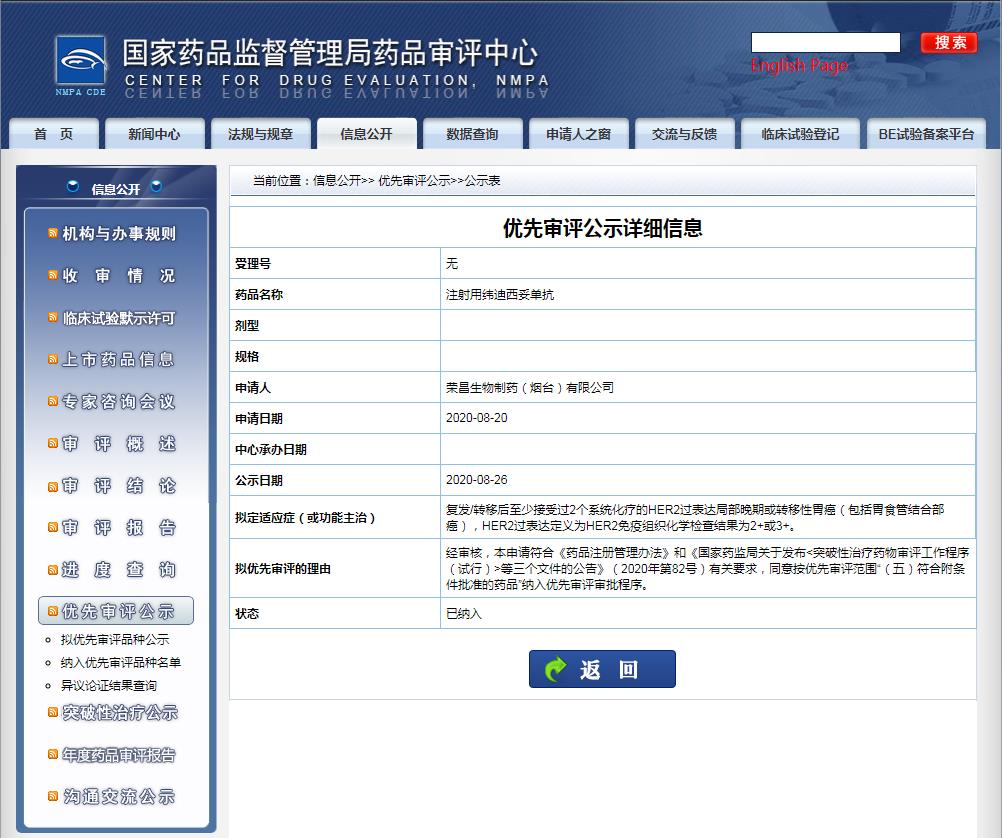
截图来源:CDE官网
在2020年8月,中国国家药品监督管理局药品审评中心(CDE)受理维迪西妥单抗的新药上市申请,并因“符合附条件批准的药品”被纳入优先审评。该药的获批适应症(或功能主治)为:复发/转后至少接受过2个系统化疗的HER2过表达局部晚期或转移性胃癌(包括胃食管结合部癌),HER2过表达定义为HER2免疫组织化学检查结果为2+或3+。
除了胃癌已经申报新药上市外,维迪西妥单抗针对尿路上皮癌、HER2低表达乳腺癌以及肺癌和胆管癌等的临床研究也在积极探索中。在2020年12月,中国国家药监局药品审评中心(CDE)受理维迪西妥单抗针对HER2过表达局部晚期或转移性尿路上皮癌患者的申请,并被纳入突破性治疗品种。

截图来源:CDE官网
据早期消息,维迪西妥单抗针对适应症为晚期或转移性胃癌以及胃食管结合部腺癌被美国食品和药物管理局(FDA)快速通道资格,除此之外,维迪西妥单抗也获得了FDA的突破性疗法认定和快速通道资格,针对治疗尿路上皮癌的申请。
局部晚期或转移性胃癌是常见的恶性肿瘤,目前缺乏新的治疗手段,临床上对新药具有重大的需求,此次NMPA批准荣昌生物维迪西妥单抗获批上市,有望为这类患者提供了新的治疗选择。


