2月3日,据CDE官网,拜耳糖尿病肾病新药「Finerenone薄膜衣片」的上市申请被CDE受理。该药今年1月份美国FDA受理其上市申请,并授予优先审评资格。

糖尿病肾病(DKD)是指由糖尿病引起的慢性肾脏疾病(CKD),临床上以持续性白蛋白和(或)肾小球滤过率(GFR)进行性下降为主要特征,可进展为终末期肾脏病(ESRD)。据国际糖尿病联盟公布的流行病学数据,2019年全球20-79岁成年人中约有4.63亿人诊断为糖尿病,其中我国糖尿病患者人数最多,高达1.16亿。DKD是终末期肾脏病的重要病因之一,据悉我国2型糖尿病患者DKD的患病率为10%-40%。
DKD发病机制复杂,血流动力学改变、炎症、纤维化、系膜扩张、内皮细胞和足细胞损伤等均可导致蛋白尿和肾功能降低。该病的治疗主要以预防为主,据2020年《糖尿病肾病多学科诊与管理专家共识》,DKD患者应严格控制血糖、血压和血脂,以及使用药物改善肾脏微循环以延缓DKD进程。
近年来,SGLT-2抑制剂(如卡格列净,恩格列净和达格列净)和GLP-1受体激动剂(如索马鲁肽)等降糖药物也被开发用于治疗DKD。其中,卡格列净已率先于2019年9月被FDA批准用于降低糖尿病肾病患者的终末期肾病、肾功能恶化、心血管死亡以及心衰住院风险。达格列净治疗糖尿病肾病的上市申请已被FDA受理,且授予优先审评资格。
Finerenone(BAY94-8862)是一种潜在first-in-class非甾体、选择性盐皮质激素受体拮抗剂(MRA),可减少盐皮质激素受体(MR)过度激活的有害影响。MR过度激活被认为通过炎症及纤维化过程,对肾损伤及心血管损伤有重要的作用,已上市的MRA如螺内酯和依普利酮被批准用于治疗高血压和心力衰竭。
2015年,Finerenone被FDA授予治疗DKD的快速通道资格(FTD)。2020年7月,拜耳宣布该药治疗患有2型糖尿病慢性肾病患者的3期临床试验FIDELIO-DKD达到主要终点。结果显示,Finerenone联合标准护理,可推迟发生肾衰竭的时间,降低因肾病死亡的风险,并且延缓肾小滤过率(eGFR)的下降速度。2021年1月12日,拜耳宣布FDA受理了该药治疗糖尿病肾病的上市申请,并授予优先审评资格,预计今年7月份就会受到FDA的回复。
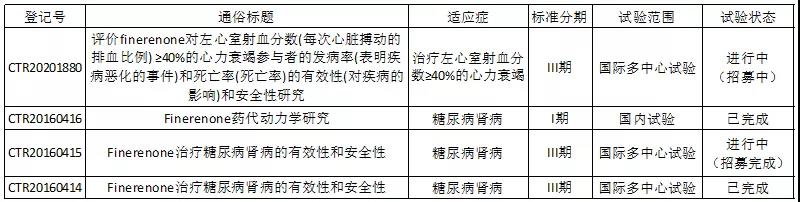
在国内,Finerenon共登记了4项临床试验,适应症包括糖尿病肾病和心力衰竭。据试验进度,推测此次申报的适应症是糖尿病肾病。
单从Finerenon在国内外上市申请的受理时间,可以看出随着我国审评制度的改革,境外药品在国内外的上市时间差越来越短,期待该药可以早日在国内获批,造福广大糖尿病肾病患者。
此外,值得一提的是,拜耳的前列腺癌新药darolutamide在国内的上市申请已于近日进入行政审批阶段,预计不日也将正式获批。该药是一款高活性的雄激素受体拮抗剂(ARI),已于2019年7月和2020年3月先后在美国和欧洲被批准用于治疗非转移性去势抵抗性前列腺癌(nmCRPC),商品名为Nubeqa。
注:本文为载,仅做分享之用,对文章观点保持中立,侵权即。
