国家药监局(NMPA)官网最新显示,安斯泰来的富马酸吉瑞替尼片上市申请(受理号:JXHS2000033)在2021年1月27日已处于“在审批”阶段,有望于近期获得NMPA批准。每日口服1次,用于治疗携带FLT3突?的复发性或难治性急性髓系白血病(AML)成人患者。
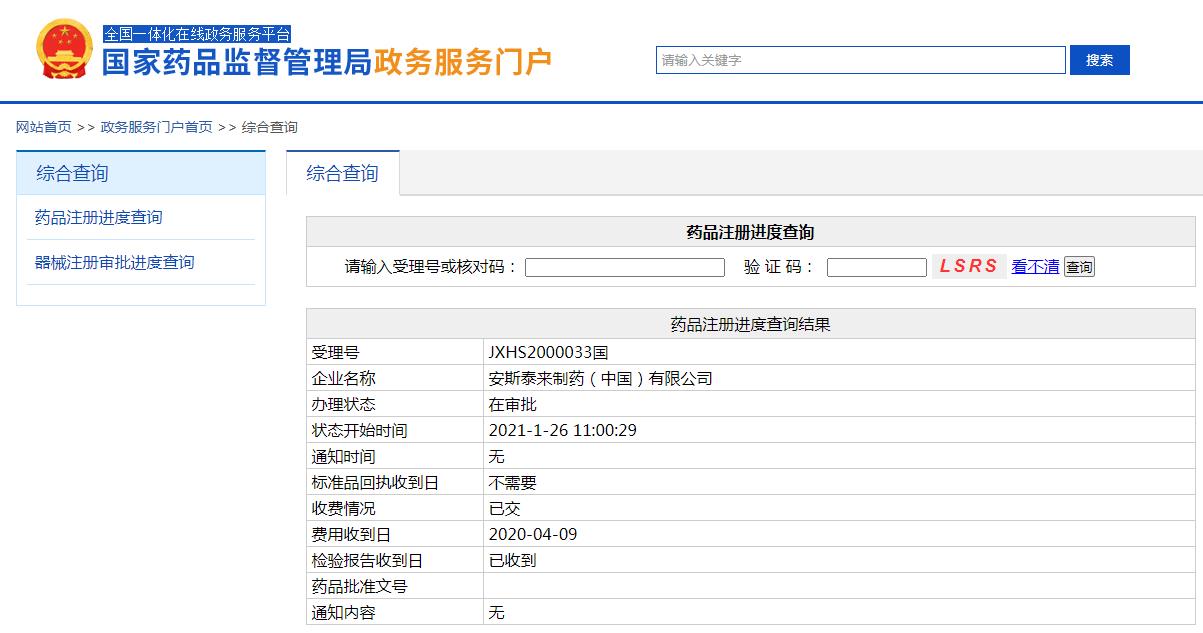
图片来源:NMPA
据悉,吉瑞替尼是安斯泰来与Kotobuki制药合作开发的一种FMS样酪氨酸激酶3(FLT3)抑制剂。
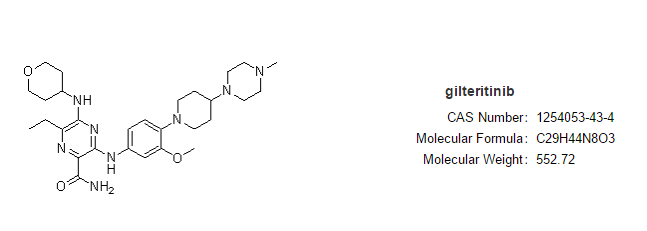
吉瑞替尼结构式
在2018年,吉瑞替尼相继在日本和美国获批上市用于治疗复发性或难治性FLT3突变急性髓系白血病成年患者,它是FDA批准的用于复发、难治性急性粒细胞白血病的FLT3抑制剂。
2020年4月10日,安斯泰来在中国提交的吉瑞替尼上市申请获得国家药品监督管理局药品审评中心(CDE)受理,并且在4月17日被拟纳入优先审评,在7月30日正式纳入优先审评。距离即将获批有不到10个月的时间。
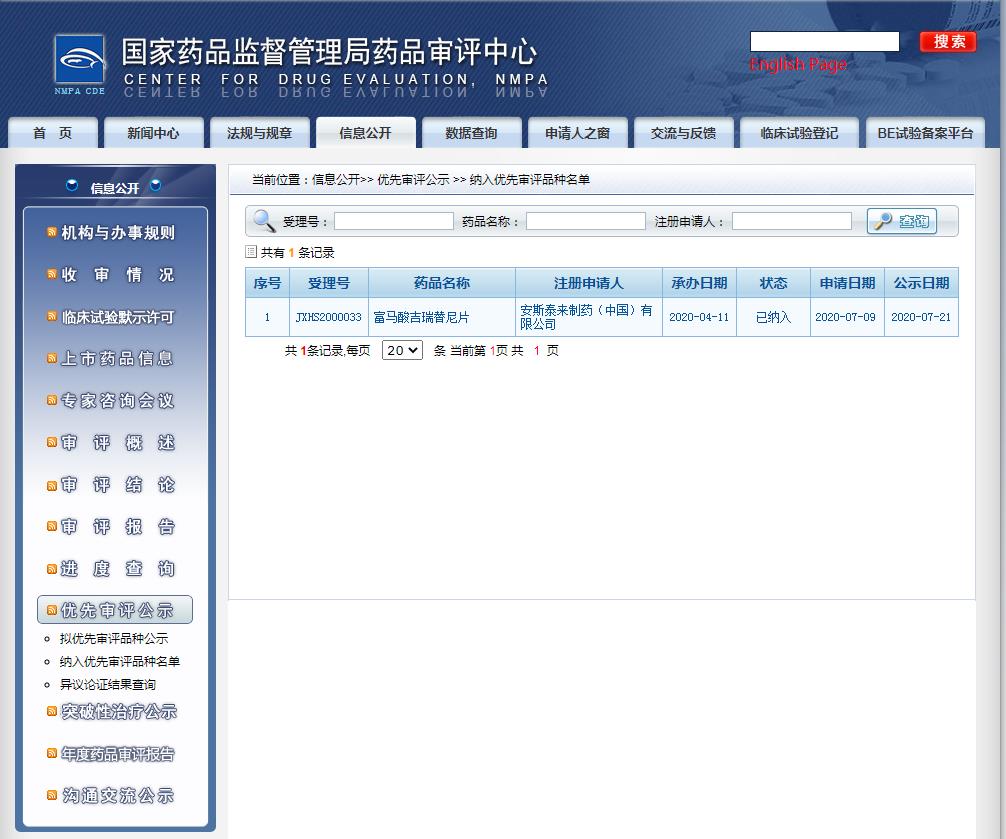

图片来源:CDE
关于急性髓系白血病
AML:acute myelocytic leukemia,即急性髓细胞白血病,是一种影响血液和骨髓的肿瘤,发病率一般情况下会随着年龄增长而增加。据统计,目前中国每年约有80000人诊断患有白血病[1]。急性髓系白血病的临床表现一般为感染、出血、浸润以及贫血。特征就是骨髓里面的异常细胞快速增长,导致影响了正常细胞的产生,成年人一般较为容易患急性骨髓性白血病。
在过去的十年中,复发性和难治性急性髓系白血病的治疗进展较为缓慢,生存期短,并发症多。 除了挽救性化疗和造血干细胞移植以外,治疗方案的选择非常有限。
FLT3突变呈阳性的急性髓系白血病患者预后差,化疗后的生存期中位数不到6个月[2]。在急性髓系白血病的治疗过程中,即使是在复发之后,FLT3突变的状态有可能发生变化。因此,确认患者FLT3的突变状态对于确定治疗方法会有帮助。
希望安斯泰来新药「吉瑞替尼」在中国早日获批上市,从而为急性系白血病患者带来新的治疗选择。
参考来源:
参考来源:
[1] GLOBOCAN Cancer Today Database, International Agency for Research on Cancer, World Health Organisation.Population Fact Sheets in 2018. Available at: http://gco.iarc.fr/today/data/factsheets/populations/160-china-factsheets.pdf. Last accessed March 2020.
[2] Perl, A et al. Gilteritinib significantly prolongs overall survival in patients with FLT3-mutated (FLT3mut+) relapsed/refractory (R/R) acute myeloid leukemia (AML): Results from the Phase III ADMIRAL trial. Presented as abstract CT184 at the AACR Annual Meeting, April 22019.
