2021年5月12日,基石药业(苏州)有限公司(以下简称“基石药业”)宣布,公司在香港地区的胃肠道间质瘤(GIST)同类精准靶向药avapritinib(阿伐替尼)上市申请已获得受理,该药物的适应症为:用于治疗携带PDGFRA D842V突变无法切除或转移性胃肠道间质瘤成人患者。
图片来源:NMPA
Avapritinib是一款KIT和PDGFRA突变激酶抑制剂,由Blueprint Medicines开发,Blueprint Medicines为基石药业的合作伙伴。
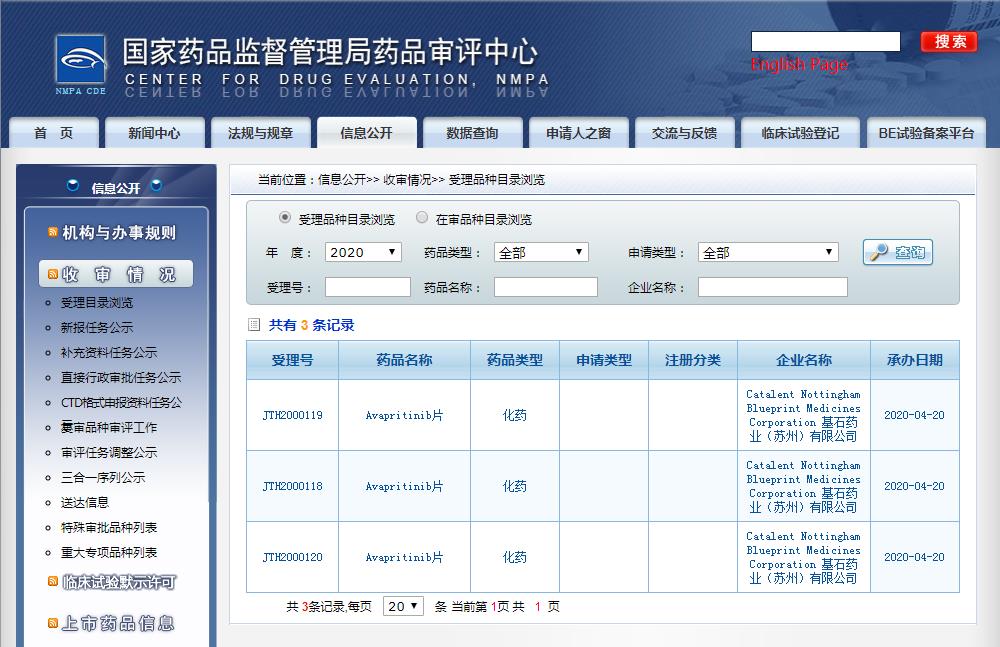
图片来源:CDE
中国国家药品监督管理局(NMPA)批准?以商品名泰吉华®上市销售,用于治疗携带PDGFRA外显子18突变 (包括PDGFRA D842V突变) 的不可切除性或转移性GIST成人患者。当前在中国大陆和台湾地区、美国、欧盟还没有批准用于其他适应症,或者其他地区的医疗监管机构还没有对avapritinib的任何适应症做出批准决定。
关于胃肠道间质瘤(GIST)
胃肠道间质瘤是发生在胃肠道的肉瘤,肉瘤是发生在骨内或源自结缔组织的肿瘤。胃肠道间质瘤起源于胃肠道壁中的细胞,并且常常发生在胃或小肠中。大多数患者的确诊年龄在50-80岁之间,胃肠道间质瘤起病比较隐秘,比较容易被常规检测手段忽略,往往在胃肠道出血、做手术或医学影像检查的时候发现,少数在肿瘤破裂或胃肠道发生梗阻后确诊,患者往往确诊时已属中晚期阶段。
在中国,每年新诊断GIST患者大概有1-1.5/10万(1.4万-2.1万)。原发胃肠道间质瘤中,大概有5%至6%新诊断为胃肠道间质瘤的患者在PDGFRA第18外显子有突变,较为常见的PDGFRA第18外显子有突变是PDGFRA D842V突变,这类患者对现有的已批准的KIT药物不敏感。
许多PDGFRA外显子18突变的GIST患者更是缺乏治疗药物,临床上迫切需要新的治疗药物来使这部分患者受到生存获益。
祝贺avapritinib的新药上市申请在香港地区获得受理,期待avapritinib能够尽快获批上市,早日惠及更多胃肠道间质瘤患者。
