2021年4月21日,石药集团提交的度恩西布胶囊(duvelisib)上市申请获国家药品监督管理局药品审评中心(CDE)正式受理,并拟纳入优先审评。用于治疗既往至少经过两次系统治疗的复发或难治性滤泡性淋巴瘤(FL)。
图片来源:CDE官网
度恩西布由Verastem公司开发,已经在2018年9月获FDA批准上市,商品名为Copiktra,是一款磷脂酰肌醇-3-激酶(PI3K)-δ和PI3K-γ口服双重抑制剂,用于治疗已经接受过至少两次前期疗法的复发/难治性慢性淋巴性白血病(CLL)和小淋巴细胞淋巴瘤(SLL)成年患者,以及至少接受过两次前期 的复系统治疗的复发/难治性滤泡性淋巴瘤(FL)成年患者。
石药集团与 Verastem于2018年9月26日签订独家产品特许及合作协议,内容有关在中国(包含香港、澳门及台湾)Copiktra的开发及商业化。
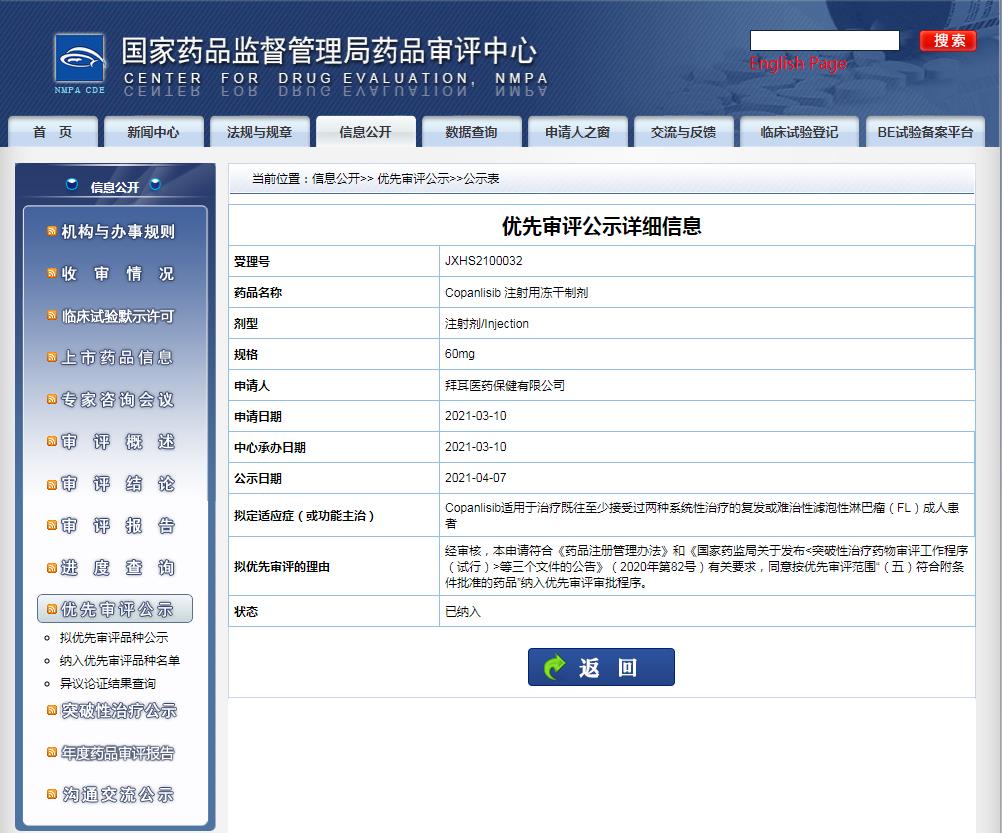
图片来源:CDE官网
此外值得注意的是,拜耳Copanlisib注射用冻干制剂在国内的上市申请已于2021年3月10日获得中国国家药品监督管理局药品审评中心(CDE)正式受理,并被纳入了优先审评,这是一款PI3K抑制剂。
关于滤泡性淋巴瘤(FL)
淋巴瘤可分为霍奇金淋巴瘤(HL)和非霍奇金淋巴瘤(NHL),非霍奇金淋巴瘤(NHL)是常见的血液系统恶性肿瘤,是十大常见癌症类型,由一组高度异质性的疾病组成,根据肿瘤细胞增殖速度和临床特点,可分为侵袭性NHL和惰性NHL。
其中,滤泡性淋巴瘤(FL)是惰性NHL常见的组织学亚型,起源于B淋巴细胞。是第2种常见的非霍奇金淋巴瘤(NHL)形式,大概占所有非霍奇金淋巴瘤(NHL)病例的17%。
滤泡性淋巴瘤多见于男性老年人,发病率有逐年增加的倾向。直到现在,确切病因尚未十分清楚,一般认为可能会与基因突变,放射线、化学药物,遗传因素、病毒及其他病原体感染、免疫因素等有关。另外,还可表现为其他系统受累或全身症状。
滤泡性淋巴瘤患者长期生存的占大多数,但是1/3的患者可转化为侵袭性的弥漫性大B细胞淋巴瘤(DLBCL),从而影响预后。滤泡性淋巴瘤病程长,容易反复复发。
当前滤泡性淋巴瘤的治疗目标是提高患者生活质量,并减少近、远期毒副反应和治疗相关并发症,降低交叉耐药的发生,尽可能使前面的治疗不影响后续治疗的选择。
