2021年2月3日,德国默克旗下公司EMD Serono宣布,美国食品和药物管理局(FDA)已批准口服MET抑制剂tepotinib(商品名:TEPMETKO)上市,用于治疗携带MET基因第14号外显子(MET ex14)跳跃突变的转移性非小细胞肺癌(NSCLC)成人患者。
Tepotinib是一种口服MET抑制剂,由德国默克自主研发,旨在抑制MET基因变异引起的致癌MET受体信号。FDA此前曾授予tepotinib突破性疗法认定,并通过实时肿瘤审评(Real-Time Oncology Review, RTOR)项目批准其上市。2020年3月,在日本获批上市,是一个获得监管部门批准用于治疗MET基因突变晚期NSCLC的口服MET抑制剂。近期,FDA还授予tepotinib孤儿药资格认定 (ODD)。
2013年7月,默克在中国向国家药品监督管理局(NMPA)递交临床申请,现如今在中国以及开展4项临床研究。
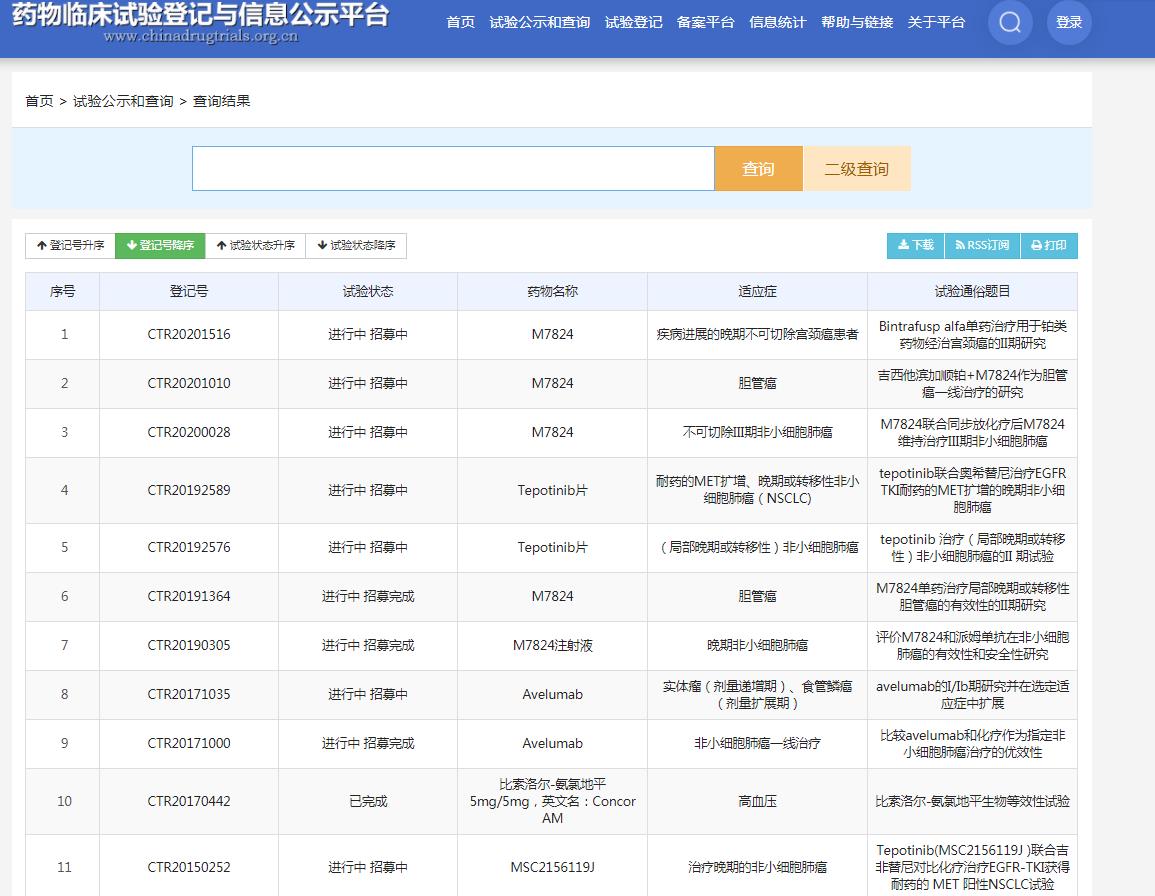

截图来源:药物临床试验登记与信息公示平台
纪念斯隆-凯特琳癌症中心胸外肿瘤科研究员、临床主任Paul K. Paik博士说:“MET ex14跳跃突变占NSCLC病例的3%——4%,这种侵袭性肺癌患者通常是老年人,预后较差。当前,临床迫切需要可以产生抗肿瘤活性以提高这种挑战性疾病患者的生活的靶向疗法。tepotinib为携带该基因突变的转移性非小细胞肺癌患者提供了新的治疗选择。”
肺癌是人体常见的的恶性肿瘤,严重威胁了人们的生命,是常见的癌症类型之一,也是癌症相关死亡的主要原因。MET信号通路的改变,包括MET第14号外显子跳跃突变和MET扩增,在许多类型癌症中被发现,包括NSCLC,这可能与肿瘤的侵袭行为和不良的临床预后有关。
祝贺默克MET抑制剂获FDA批准上市,它的到来将给非小细胞肺癌患者带来新的治疗选择和希望。
