在今年的8月2日,中国国家药品监督管理局(NMPA)官网显示,百济神州(北京)生物科技有限公司(以下简称:百济神州)申报的达妥昔单抗β(Dinutuximab beta,曾又名:迪妥昔单抗)注射液上市申请已处于“在审批”状态,有望在近期获得NMPA上市批准。
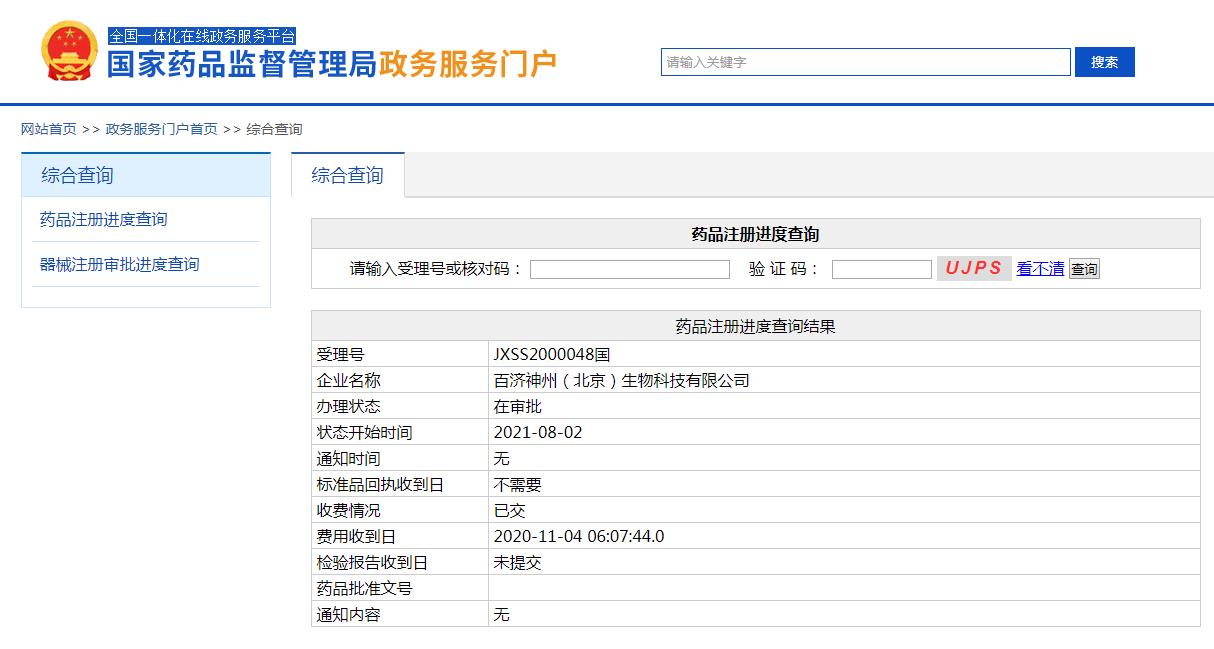
截图来源:NMPA官网
此次达妥昔单抗β获批的两项适应症为:1) 治疗伴或不伴有残留病灶的复发性或难治性神经母细胞瘤;2) 治疗≥12月龄的高危神经母细胞瘤患者,这些患者既往接受过诱导化疗且至少获得部分缓解,并且随后进行过清髓性治疗和干细胞移植治疗。
2015年3月,达妥昔单抗β获得美国FDA批准,这是由EUSA Pharma开发的一款GD2单抗,是美国FDA批准的一个治疗儿童高危神经母细胞瘤的药物;2015年8月在欧盟获批,商品名为Qarziba。
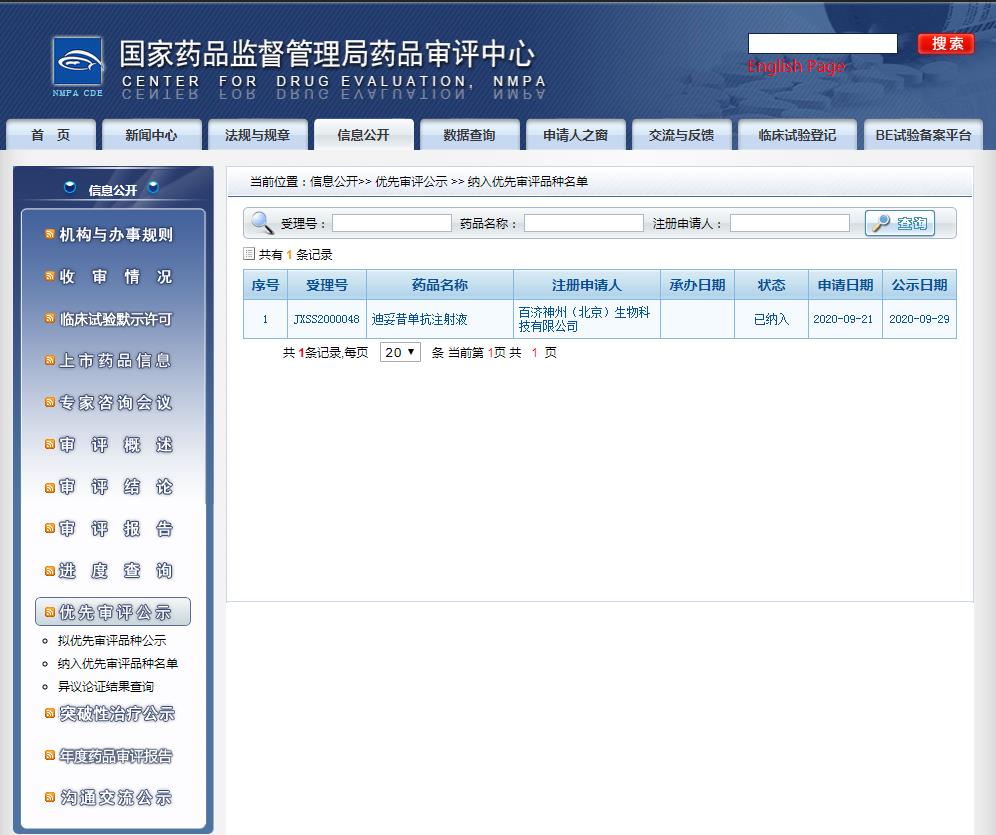
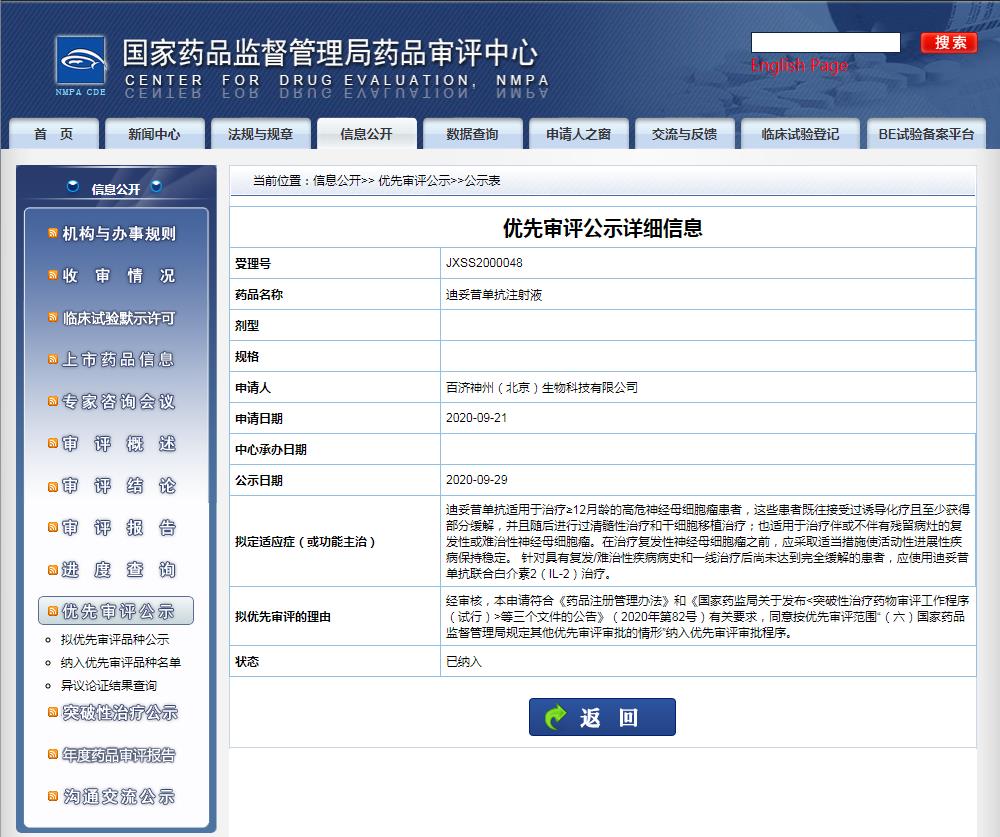
截图来源:CDE官网
根据此前消息显示,达妥昔单抗β的上市申请获中国国家药监局药品审评中心(CDE)受理,并纳入优先审评资格。
2020年1月,百济神州与EUSA Pharma达成合作,获得了在大中华区开发和商业化包括达妥昔单抗β在内的2产品的权利。另一款产品目前处于申报上市阶段,是抗IL-6单抗司妥昔单抗。
关于神经母细胞瘤(NB)
神经母细胞瘤(neuroblastoma,NB)占儿童恶性肿瘤的8%10%,是儿童常见的颅外神经系统恶性肿瘤之一。小儿神经母细胞瘤属于比较罕见的疾病,我国年发病率低于 5/100 万。
神经母细胞瘤临床表现多种多样,症状无特异性,早期诊断十分困难,容易漏诊,在诊时往往易误诊为其它疾病。神经母细胞瘤来源于未分化的交感神经节细胞,故凡有胚胎性交感神经节细胞的部位,都可发生肿瘤。常见的原发部位是肾上腺,大概1%的患者没有发现原发肿瘤。神经母细胞瘤全身多发转移,包括淋巴结、骨髓、骨骼等,少数情况下,也可能会转移至肺部和颅内。
神经母细胞瘤是一组临床表现及预后差异很大的疾病,会对患者及其家属带来很大的痛苦。尽管目前的疾病治疗手段在不断进步,但现在依然存在未被满足的治疗需求。
希望达妥昔单抗β能够早日获批上市,为神经母细瘤患者带来更多的治疗选择。
