近日,国家药品监督管理局(NMPA)药品审评中心(CDE)显示,恒瑞医药CDK4/6 抑制剂、君实生物抗PD-1被CDE拟纳入突破性治疗品种!

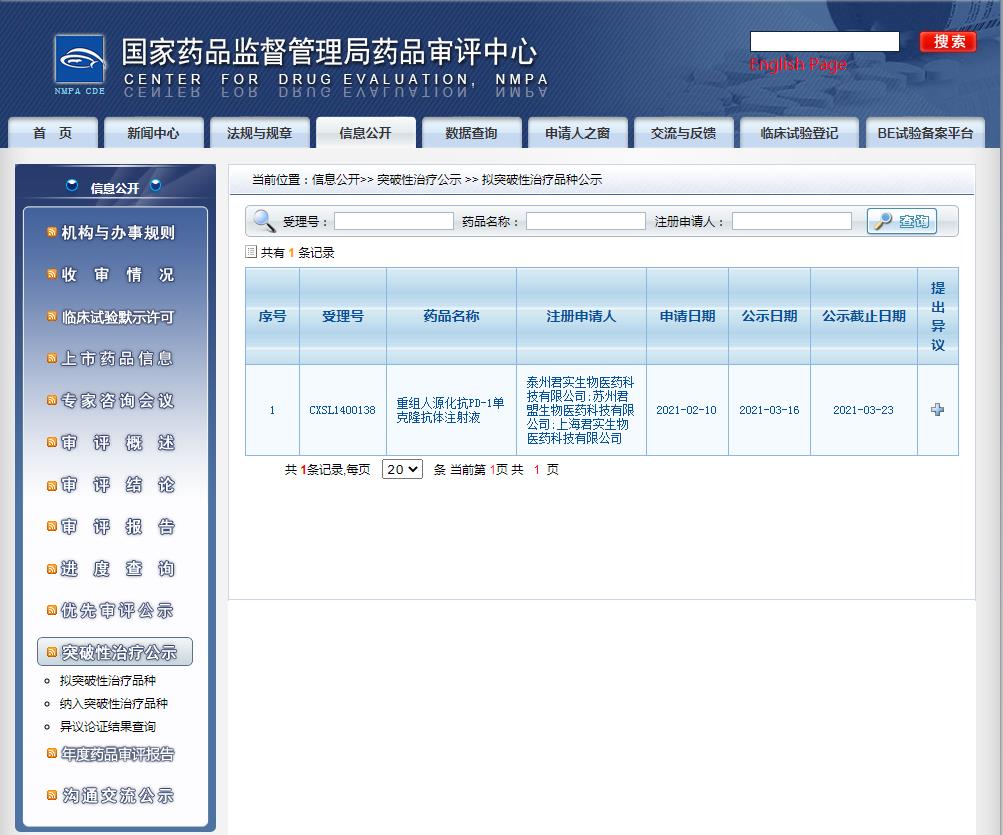
片来源:CDE官网
关于恒瑞医药CDK4/6 抑制剂
SHR6390片这一次拟纳入突破性疗法适应症为联合氟维司群用于经内分泌治疗后进展的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的复发或转移性乳腺癌患者的治疗。SHR6390片,是恒瑞医药开发的一种口服、选择性的小分子 CDK4/6 抑制剂。
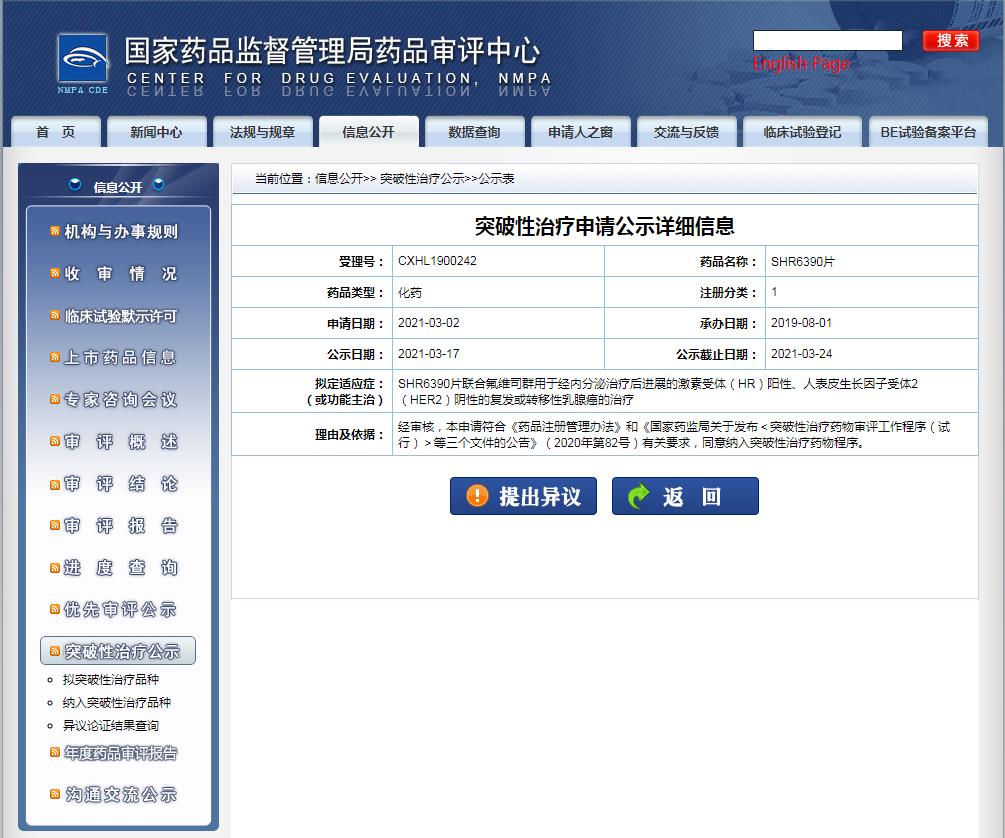
图片来源:CDE官网
目前,已经有辉瑞和齐鲁的哌柏西利胶囊以及礼来的阿贝西利片在国内获批上市,而恒瑞的SHR6390片有望成为在中国上市的第3款CDK 4/6抑制剂。
关于君实生物抗PD-1
君实生物的PD1特瑞普利单抗注射液这一次拟纳入突破性疗法适应症是一线治疗晚期黏膜黑色素瘤。这一项适应症在1月24日的时候也获得了FDA授予的快速通道资格认定。
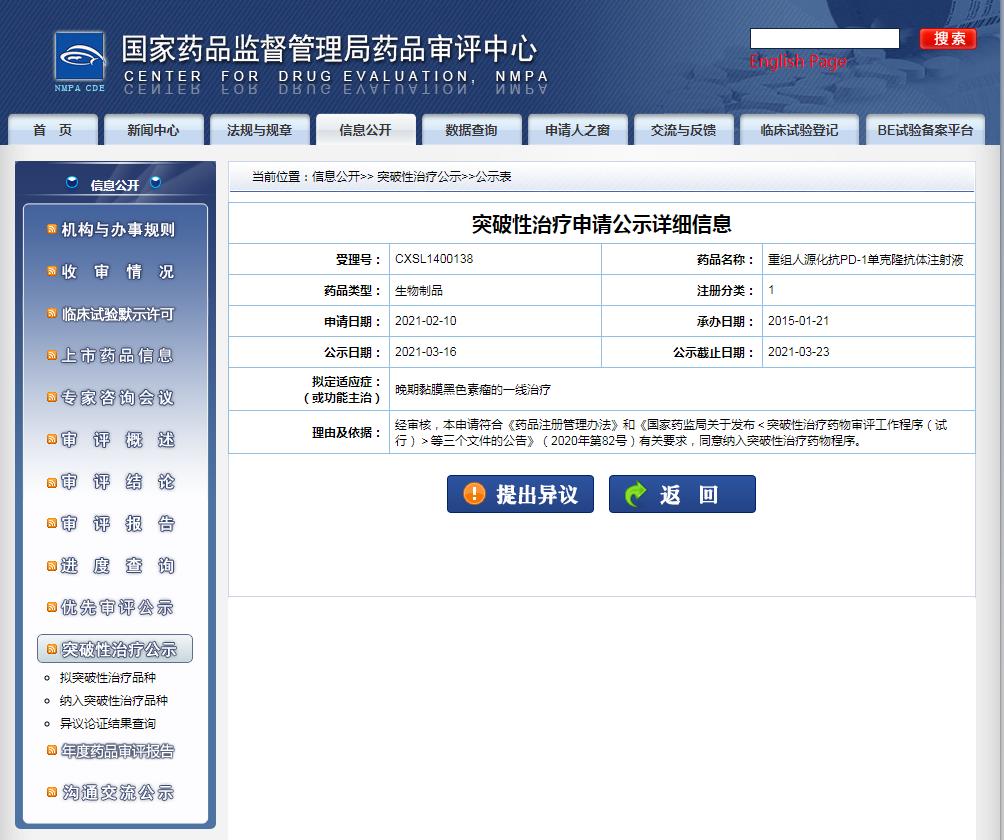
图片来源:CDE官网
值得我们注意的是,特瑞普利单抗的第一个获批上市的适应症是:治疗既往接受全身系统治疗失败后不可切除或转移性黑色素瘤,并获得了2019 年和 2020 年《中国临床肿瘤学会(CSCO)黑色素瘤诊疗指南》推荐。
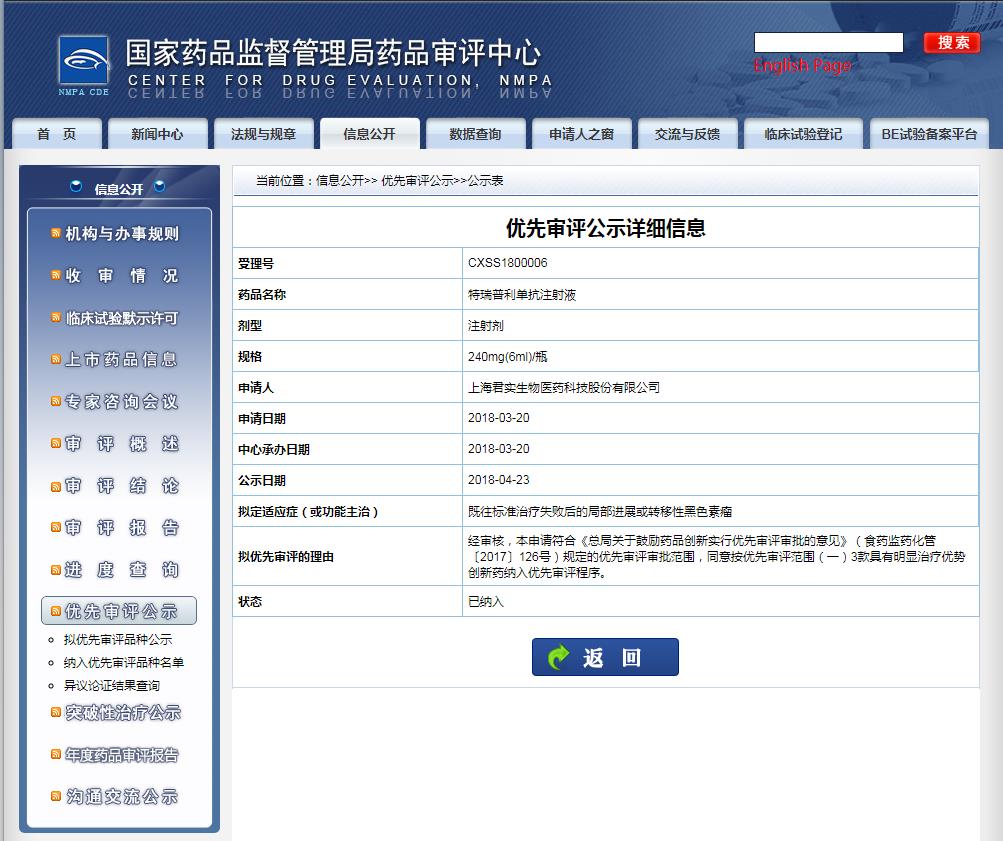
图片来源:CDE官网
据了解,黏膜黑色素瘤是黑色素瘤的亚型之一。它对传统化学疗法不敏感,对单药免疫疗法的反应也非常有限。特瑞普利单抗比较早就开始探索抗 PD-1 单抗和VEGFR 抑制剂在粘膜黑色素瘤中的PD-1抑制剂的联合应用了。
